EN ESTA PÁGINA: obtendrá información sobre los diferentes tratamientos que los médicos usan en las personas con este cáncer de mama. Use el menú para ver otras páginas.
En esta sección, se explican los tipos de tratamientos, también conocidos como terapias, que constituyen el estándar de atención para el cáncer de mama de avance local o en estadio temprano. “Estándar de atención” significa los mejores tratamientos conocidos. Al tomar decisiones relacionadas con el plan de tratamiento, se le recomienda que hable con su médico acerca de si existe la opción de participar en ensayos clínicos. Un ensayo clínico es un estudio de investigación que prueba un nuevo enfoque al tratamiento. A través de los ensayos clínicos, los médicos averiguan si un nuevo tratamiento es seguro, eficaz y posiblemente mejor que el tratamiento estándar. Los ensayos clínicos pueden evaluar un nuevo fármaco y con qué frecuencia se debe administrar, una nueva combinación de tratamientos estándares o nuevas dosis de fármacos estándares u otros tratamientos. Algunos ensayos clínicos también evalúan dar menos tratamiento farmacológico o de radioterapia o hacer una cirugía menos extensa de la que se realiza habitualmente como estándar de atención. Los ensayos clínicos son una opción para todos los estadios del cáncer. Su médico puede ayudarle a considerar todas sus opciones de tratamiento. Obtenga más información sobre los ensayos clínicos en las secciones Acerca de los ensayos clínicos y Últimas investigaciones de esta guía.
Cómo se trata el cáncer de mama
En la atención del cáncer, médicos especialistas en diferentes áreas del tratamiento para el cáncer—como cirugía, radioncología y oncología médica—trabajan en conjunto con radiólogos y patólogos para crear un plan de tratamiento integral para la paciente que combine distintos tipos de tratamientos. Esto se denomina equipo multidisciplinario (en inglés). Los equipos de atención del cáncer incluyen una variedad de otros profesionales de atención médica, por ejemplo, auxiliares médicos, enfermeros profesionales, enfermeros de oncología, trabajadores sociales, farmacéuticos, asesores genéticos, nutricionistas, terapeutas y otros. En el caso de las personas mayores de 65 años, en la atención también puede intervenir un oncólogo geriátrico o un geriatra. Pregunte a los miembros de su equipo de tratamiento quién es el contacto principal para hacer preguntas sobre la planificación de fechas y el tratamiento, quién está a cargo durante las diferentes partes del tratamiento, cómo se comunican entre los equipos y si hay un contacto que pueda ayudar con la comunicación entre las especialidades, como un enfermero de enlace. Esto puede cambiar con el transcurso del tiempo conforme su atención médica necesite modificaciones.
Un plan de tratamiento es un resumen de su cáncer y el tratamiento planeado contra este. Tiene como fin brindar información básica sobre sus antecedentes médicos a cualquier médico que lo atienda durante su vida. Antes de que comience el tratamiento, pida al médico una copia de su plan de tratamiento. También puede proporcionarle a su médico una copia del formulario del Plan de tratamiento de la American Society of Clinical Oncology (en inglés) para completarlo.
La biología y el comportamiento del cáncer de mama influyen en el plan de tratamiento. Algunos tumores son más pequeños, pero crecen rápidamente, mientras que otros son más grandes y crecen con lentitud. Las opciones y recomendaciones de tratamiento son muy personalizadas y dependen de varios factores, entre ellos:
-
El subtipo de tumor, que incluye el estado de los receptores de hormonas (RE, RP), el estado del HER2 y el estado de los ganglios (consulte Introducción).
-
El estadio del tumor.
-
Las pruebas genómicas, como las series de pruebas para múltiples genes Oncotype DX™ o MammaPrint™, si corresponde (consulte Diagnóstico).
-
La edad del paciente, el estado de salud general, el estado de la menopausia y sus preferencias.
-
La presencia de mutaciones conocidas en los genes heredados del cáncer de mama, como BRCA1 o BRCA2, según los resultados de las pruebas genéticas.
Si bien su equipo de atención del cáncer de mama adaptará el tratamiento específicamente para cada paciente y tumor, que se denomina “medicina personalizada”, hay algunos pasos generales para tratar el cáncer de mama de avance local y en estadio temprano.
Tanto en el caso del carcinoma ductal in situ (CDIS) como en el cáncer de mama invasivo de estadio temprano, los médicos por lo general recomiendan cirugía para extirpar el tumor. A fin de asegurarse de extirpar todo el tumor, el cirujano también extirpará una pequeña área de tejido normal que rodea al tumor, denominado margen. Aunque el objetivo de la cirugía es extirpar todo el cáncer visible en la mama, pueden quedar células microscópicas. En algunas situaciones, esto significa que podría ser necesaria otra cirugía para extirpar las células cancerosas restantes. Existen diferentes maneras de buscar células microscópicas que garanticen un margen limpio. También es posible que las células microscópicas estén presentes fuera de la mama, por lo que a menudo se recomienda el tratamiento sistémico con medicamentos después de la cirugía, tal como se describe a continuación.
Para los cánceres más grandes o para aquellos que crecen más rápidamente, los médicos pueden recomendar un tratamiento sistémico con quimioterapia, inmunoterapia o terapia hormonal antes de la cirugía, que se denomina “terapia neoadyuvante”. Existen varios beneficios de recibir tratamientos farmacológicos antes de la cirugía:
-
La cirugía podría ser más fácil de realizar debido a que el tumor es más pequeño.
-
Su médico puede descubrir si ciertos tratamientos son eficaces para el cáncer.
-
Es posible que usted pruebe un nuevo tratamiento mediante un ensayo clínico.
-
Si tiene alguna enfermedad microscópica a distancia, la terapia farmacológica que circula por el cuerpo la tratará antes.
-
Las personas que pueden haber necesitado una mastectomía podrían someterse a una cirugía con conservación de la mama (lumpectomía) si el tumor se reduce lo suficiente antes de la cirugía.
Después de la cirugía, el siguiente paso en el control del cáncer de mama en estadio temprano consiste en reducir el riesgo de recurrencia y tratar de eliminar cualquier célula cancerosa restante en el cuerpo. Estas células cancerosas son indetectables con las pruebas actuales, pero se cree que son las responsables de la recurrencia del cáncer, ya que pueden crecer con el tiempo. El tratamiento que se administra después de la cirugía se denomina “terapia adyuvante”. Las terapias adyuvantes incluyen radioterapia, quimioterapia, terapia dirigida, inmunoterapia o terapia hormonal (consulte a continuación para obtener más información sobre estos tratamientos).
La necesidad de la terapia adyuvante depende de la posibilidad de que queden células cancerosas en la mama o en el cuerpo o de que un tratamiento específico funcione para tratar el cáncer. Si bien la terapia adyuvante disminuye el riesgo de recurrencia, no necesariamente lo elimina.
Junto con la determinación del estadio, existen otras herramientas que pueden ayudar a determinar el pronóstico y ayudarlos a usted y a su médico a tomar decisiones acerca de la terapia adyuvante. Según el subtipo de cáncer de mama, incluye pruebas que pueden predecir el riesgo de recurrencia al examinar el tejido tumoral (por ejemplo, Oncotype Dx™ o MammaPrint™; consulte Diagnóstico). Estas pruebas también pueden ayudar al médico a comprender mejor si la quimioterapia ayudará a reducir la recurrencia.
Los casos en que no es posible realizar una cirugía para extirpar el cáncer se denominan “inoperables”. El médico entonces recomendará otras formas de tratamiento para el cáncer. Es probable que se utilice quimioterapia, inmunoterapia, terapia dirigida, radioterapia o terapia hormonal para reducir el tamaño del cáncer.
Para los casos de cáncer recurrente, las opciones de tratamiento dependen de cómo se trató el cáncer en un comienzo y de las características del cáncer antes mencionadas, como RE, RP y HER2.
Tómese el tiempo para obtener información sobre todas sus opciones de tratamiento y asegúrese de hacer preguntas sobre cosas que no estén claras. Hable con su médico acerca de los objetivos de cada tratamiento y lo que puede esperar mientras recibe el tratamiento. Estos tipos de conversaciones se denominan “toma de decisiones compartida”. La toma de decisiones compartida es cuando usted y sus médicos trabajan juntos para elegir tratamientos que se ajusten a los objetivos de su atención. La toma de decisiones compartida es especialmente importante en los casos de cáncer de mama, ya que existen diferentes opciones de tratamiento. Antes de comenzar cualquier tratamiento, también es importante consultar con la aseguradora para asegurarse de que cubra el tratamiento previsto.
Las personas con más de 65 años de edad pueden beneficiarse de someterse a una evaluación geriátrica antes de planificar el tratamiento. Averigüe qué implica una evaluación geriátrica y cómo puede ayudar a las personas mayores de 65 años con cáncer.
Obtenga más información sobre la toma de decisiones sobre el tratamiento.
A continuación, se describen los tipos de tratamiento más frecuentes para el cáncer de mama de avance local o en estadios tempranos. Su plan de atención también incluye tratamiento contra síntomas y efectos secundarios, una parte importante de la atención del cáncer. Tenga en cuenta que esta información se basa en los estándares de atención para el cáncer de mama en los Estados Unidos. Las opciones de tratamiento pueden variar de un lugar a otro.
Cirugía
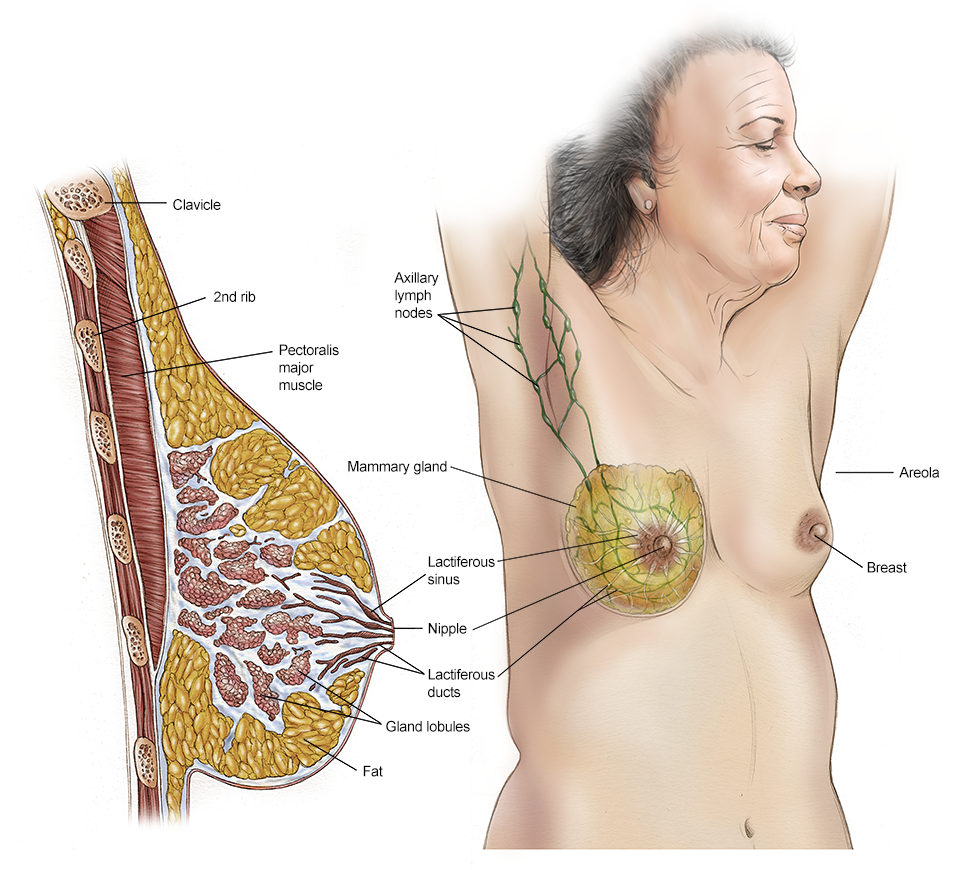
La cirugía es la extirpación del tumor y de parte del tejido circundante sano durante una operación. La cirugía también se utiliza para evaluar los ganglios linfáticos cercanos axilares, que se encuentran debajo del brazo. Un cirujano oncólogo es un médico que se especializa en el tratamiento para el cáncer mediante la cirugía. Obtenga más información sobre los aspectos básicos de la cirugía para el cáncer.
La elección de la cirugía no afecta la necesidad de terapia con medicamentos, como quimioterapia, terapia hormonal o terapia dirigida (consulte a continuación). Las farmacoterapias se administran en función de las características del tumor, no del tipo de cirugía que se le realiza.
En general, cuanto más pequeño es el tumor, más opciones quirúrgicas tienen las pacientes (en inglés). Los tipos de cirugía por cáncer de mama incluyen los siguientes:
-
Lumpectomía. Consiste en la extirpación del tumor y de un pequeño margen sin cáncer de tejido sano alrededor del tumor. Queda la mayor parte de la mama. En el caso del cáncer invasivo, a menudo se recomienda la radioterapia en el tejido mamario restante después de la cirugía, especialmente en pacientes más jóvenes, pacientes con tumores negativos para receptores hormonales y pacientes con tumores más grandes. Para el CDIS, generalmente se administra radioterapia después de la cirugía. La lumpectomía también puede denominarse cirugía con conservación de la mama, mastectomía parcial, cuadrantectomía o mastectomía segmental.
-
Mastectomía. Es la extirpación quirúrgica de toda la mama. Existen diversos tipos de mastectomía. Hable con su médico sobre la posibilidad de conservar la piel, lo que se denomina mastectomía con conservación de la piel, o si se puede conservar el pezón, lo que se denomina mastectomía con conservación del pezón o mastectomía con conservación total de la piel. Su médico también considerará el tamaño del tumor en comparación con el tamaño de su mama para determinar el mejor tipo de cirugía para usted. Se puede recomendar radioterapia después de la mastectomía. Obtenga más información sobre el ejercicio después de una mastectomía (en inglés).
Extracción, análisis y tratamiento de ganglios linfáticos
Las células cancerosas de algunos cánceres pueden encontrarse en los ganglios linfáticos axilares. Saber si alguno de los ganglios linfáticos cercanos a la mama contiene cáncer puede proporcionar información útil para determinar el tratamiento y el pronóstico.
-
Biopsia del ganglio linfático centinela. En una biopsia del ganglio linfático centinela (también denominada biopsia del ganglio centinela), el cirujano busca y extirpa entre 1 y 3 ganglios linfáticos o más de debajo del brazo que reciben el drenaje linfático de la mama. Este procedimiento no es una opción cuando el médico ya sabe, en función de la evaluación clínica, que los ganglios linfáticos tienen cáncer. Más bien, puede ser una opción para las pacientes sin evidencia clínica obvia de compromiso de ganglios linfáticos. Este procedimiento ayuda a evitar la extirpación de una mayor cantidad de ganglios linfáticos mediante un vaciamiento de los ganglios linfáticos axilares (consulte a continuación) para pacientes cuyos ganglios linfáticos centinela mayormente no presentan cáncer. El procedimiento en los ganglios linfáticos más pequeños ayuda a reducir el riesgo de varios efectos secundarios posibles. Esos efectos secundarios incluyen hinchazón del brazo denominada linfedema, entumecimiento, movimiento del brazo y problemas con el rango de movimiento del hombro. Estos son problemas duraderos que pueden afectar gravemente la calidad de vida de una persona. Es importante mencionar el riesgo de linfedema aumenta con la cantidad de ganglios linfáticos y de vasos linfáticos que se extirparon o dañaron durante el tratamiento para el cáncer. Esto significa que las personas que se someten a una biopsia del ganglio linfático centinela tienden a desarrollar linfedema con menos probabilidad de las que se someten a una linfadenectomía axilar (consulte a continuación).
Su médico puede recomendar la obtención de imágenes de los ganglios linfáticos con una ecografía o una biopsia guiada por imagen de los ganglios linfáticos antes de una biopsia del ganglio linfático centinela para averiguar si el cáncer se ha extendido allí (consulte Diagnóstico). Esto se suele hacer si los ganglios linfáticos se pueden palpar durante el examen clínico o si se está sometiendo a un tratamiento con quimioterapia antes de la cirugía. Sin embargo, la American Society of Clinical Oncology no recomienda hacer esto si su cáncer es pequeño y sus ganglios linfáticos no pueden ser palpados durante el examen clínico.
Para detectar el ganglio linfático centinela, el cirujano generalmente inyecta un marcador radiactivo y, en ocasiones, un tinte detrás del pezón o en el área circundante a este. La inyección, que puede causar algunas molestias, dura aproximadamente 15 segundos. El tinte o el trazador se trasladan a los ganglios linfáticos, llegando primero al ganglio centinela. Si se utiliza un marcador radiactivo, este emitirá radiación, lo que ayuda al cirujano a encontrar el ganglio linfático. Si se usa un tinte, el cirujano puede encontrar el ganglio linfático cuando se torna de color azul.
Posteriormente, el patólogo examina los ganglios linfáticos para detectar la presencia de células cancerosas. Las investigaciones han demostrado que, si el ganglio linfático centinela no tiene cáncer, hay una gran probabilidad de que los ganglios linfáticos restantes tampoco lo tengan. Eso significa que no deben extirparse otros ganglios linfáticos. Si se detecta cáncer en el ganglio linfático centinela, la necesidad de otras cirugías para extirpar más ganglios linfáticos depende de la situación específica. Por ejemplo, si solo 1 o 2 ganglios linfáticos centinela tienen cáncer y usted planifica someterse a una lumpectomía y hacer radioterapia en toda la mama, es posible que no sea necesario realizar un vaciamiento de los ganglios linfáticos axilares.
En general, para la mayoría de las personas con cáncer de mama en estadio temprano con tumores que pueden extirparse con cirugía y cuyos ganglios linfáticos axilares no están agrandados, la biopsia de ganglios linfáticos centinela es el estándar de atención. Sin embargo, en determinadas situaciones, puede ser apropiado no someterse a ninguna cirugía axilar. Debe hablar con su cirujano sobre si este puede ser el enfoque adecuado para usted.
-
Vaciamiento de los ganglios linfáticos axilares. En el vaciamiento de los ganglios linfáticos axilares, el cirujano extirpa diversos ganglios linfáticos que están debajo del brazo. Luego, un patólogo los examina para detectar la presencia de células cancerosas. La cantidad real de ganglios linfáticos extirpados varía de persona a persona. Las personas que se someten a una lumpectomía y a radioterapia que tienen un tumor más pequeño y no más de 2 ganglios linfáticos centinela que presentan cáncer podrían evitar el vaciamiento total de los ganglios linfáticos axilares. Esto ayuda a reducir el riesgo de efectos secundarios y no disminuye la supervivencia.
Normalmente, los ganglios linfáticos no se evalúan en el caso de personas con CDIS y cáncer no invasivo, debido a que el riesgo de que el cáncer se haya diseminado es muy bajo. Sin embargo, en pacientes con diagnóstico de CDIS que eligen realizarse o necesitan una mastectomía, el cirujano puede considerar la posibilidad de realizar una biopsia del ganglio linfático centinela. Si se detecta algo de cáncer invasivo con el CDIS durante la mastectomía, lo que puede suceder ocasionalmente, será necesario evaluar los ganglios linfáticos. Sin embargo, por lo general, no se puede realizar una biopsia del ganglio linfático centinela si la mama ya se ha extirpado con mastectomía. En esa situación, se puede recomendar una disección de ganglio linfático axilar.
La mayoría de las personas con cáncer de mama invasivo se someterán a la biopsia del ganglio linfático centinela o al vaciamiento de los ganglios linfáticos axilares. Para la mayoría de las personas menores de 70 años con cáncer de mama en estadio temprano, se utilizará una biopsia del ganglio linfático centinela para determinar si hay cáncer en los ganglios linfáticos axilares, ya que esta información se utiliza para tomar decisiones sobre el tratamiento. Muchas pacientes de 70 años o más con enfermedad positiva para receptores hormonales pequeños y HER2 negativo y sin cáncer clínicamente aparente en los ganglios linfáticos pueden evitar una evaluación de los ganglios linfáticos, ya que los resultados pueden no cambiar las recomendaciones para las terapias con medicamentos o radioterapia. A las pacientes mayores de 70 años con tumores positivos para receptores hormonales y negativos para HER2, con otros tipos de cáncer de mama o con ganglios linfáticos clínicamente aparentes se les recomendará, en general, la evaluación de los ganglios linfáticos axilares. Las pacientes deben hablar con su médico sobre las recomendaciones para su situación específica.
Sin quimioterapia antes de la cirugía y sin cáncer en los ganglios linfáticos centinela. Para la mayoría de las personas en esta situación, la American Society of Clinical Oncology no recomienda una linfadenectomía axilar. A un pequeño grupo de pacientes con tumores localizados en lugares específicos o con características de alto riesgo se les puede ofrecer radioterapia en los ganglios linfáticos.
Sin quimioterapia antes de la cirugía, pero con cáncer en los ganglios linfáticos centinela. Si existe cáncer en 1 o 2 ganglios linfáticos centinela, entonces generalmente se puede evitar otra cirugía ganglionar si la paciente planea someterse a una lumpectomía y recibir radiación. Si hay cáncer en 3 o más ganglios linfáticos centinela, la American Society of Clinical Oncology recomienda otra cirugía ganglionar.
La quimioterapia se administra antes de la cirugía. El tratamiento para las personas que han recibido quimioterapia antes de la cirugía depende de si la quimioterapia ha destruido el cáncer en los ganglios linfáticos. Por lo tanto, después de la quimioterapia, las pacientes a menudo se vuelven a clasificar mediante una biopsia del ganglio linfático centinela. Sin embargo, este no siempre es el caso. Si los exámenes de diagnóstico por imágenes o los exámenes físicos sugieren la presencia de ganglios linfáticos anormales, la paciente debe someterse a una disección de ganglios linfáticos axilares en su lugar.
-
Si no había evidencia de cáncer en los ganglios linfáticos ni antes ni después de la quimioterapia, no se recomienda la radioterapia en el área de los ganglios linfáticos.
-
Si había indicios de cáncer en los ganglios linfáticos antes de la quimioterapia y ya no hay evidencia de cáncer en los ganglios linfáticos después de la quimioterapia, se recomienda la radioterapia en el área de los ganglios linfáticos.
-
Si hay indicios de cáncer en los ganglios linfáticos después de la quimioterapia, se recomiendan tanto la linfadenectomía axilar como la radioterapia en el área de los ganglios linfáticos.
Esta información se basa en las directrices de Ontario Health (Cancer Care Ontario) y de la American Society of Clinical Oncology, “Management of the Axilla in Early-Stage Breast Cancer” (Manejo de la axila en el cáncer de mama en estadio temprano). Tenga en cuenta que este enlace lo llevará a otro sitio web en inglés de la American Society of Clinical Oncology.
Cirugía reconstructiva (plástica)
Es recomendable que las pacientes que tengan una mastectomía o lumpectomía consideren la reconstrucción de las mamas (en inglés). Es una cirugía para recrear una mama haciendo uso de tejido tomado de otra parte del cuerpo o implantes sintéticos. La reconstrucción generalmente la realiza un cirujano plástico. Una reconstrucción hecha al mismo tiempo que la mastectomía se denomina reconstrucción inmediata. También puede someterse a ella más adelante, lo cual se denomina reconstrucción tardía.
Para algunas pacientes que se someten a una lumpectomía, la reconstrucción para que ambas mamas tengan un aspecto similar se denomina cirugía oncoplástica. Este tipo de cirugía puede ser realizada por el cirujano de mamas.
Las técnicas analizadas a continuación son usadas habitualmente para formar una nueva mama.
Implantes. Un implante mamario usa moldes rellenos con salina o con gel de silicona para reconstruir la mama. La parte externa de un implante relleno con solución salina está fabricada de silicona y se rellena con salina estéril, es decir, solución salina. Los implantes rellenos con gel de silicona tienen silicona en lugar de solución salina. Se plantearon inquietudes anteriores que podrían estar asociadas con trastornos del tejido conjuntivo, pero no se ha encontrado evidencia clara de esto. Antes de hacer implantes permanentes, es posible que a una paciente se le coloque un expansor de tejido que generará el tamaño correcto en la cavidad para el implante. Los implantes se pueden colocar por encima o por debajo del músculo pectoral. Hable con su médico acerca de los beneficios y los riesgos de los implantes de silicona en comparación con los implantes de solución salina. La vida útil de un implante depende de la persona. Sin embargo, algunas personas nunca necesitan reemplazarlos. Otros factores importantes que se deben considerar al elegir implantes incluyen lo siguiente:
-
Los implantes de solución salina, a veces, “se ondulan” en la parte superior o cambian con el paso del tiempo, pero muchas personas no ven esto como algo lo suficientemente molesto como para reemplazarlos.
-
Los implantes de solución salina se sienten diferentes al tacto de los implantes de silicona. A menudo, son más firmes al tacto que los implantes de silicona. Si se llenan excesivamente, pueden ser más firmes, pero también pueden sentirse más apretados si no están llenos.
Es posible que existan problemas con los implantes. Es posible que algunas personas tengan problemas con la forma o el aspecto. Los implantes pueden romperse o desgarrarse, causar dolor y generar tejido cicatricial alrededor del implante o se pueden infectar. Los implantes también se han vinculado en raras ocasiones a otros tipos de cáncer, incluido un tipo denominado “linfoma anaplásico de células grandes asociado al implante mamario” (LACG-IM). Dado que el riesgo de desarrollar LACG-IM es bajo, la Food and Drug Administration (FDA, Administración de Alimentos y Medicamentos) de los EE. UU. no recomienda la extracción de implantes mamarios texturizados ni de expansores de tejido, a menos que haya síntomas. Aunque estos problemas son poco comunes, hable con el médico acerca de los riesgos.
Procedimientos de colgajos de tejido. Estas técnicas usan músculos y tejidos de otras partes del cuerpo para reconstruir la mama. La cirugía de colgajo de tejido puede realizare con un “colgajo de pedículo”, lo que supone que se traslade tejido de la espalda o del vientre al pecho sin cortar los vasos sanguíneos. “Colgajo libre” hace referencia al procedimiento en que los vasos sanguíneos se cortan y el cirujano debe unir el tejido trasladado con los nuevos vasos sanguíneos en el pecho. Existen varios procedimientos con colgajos:
-
Colgajo musculocutáneo de recto abdominal transverso (TRAM, por sus siglas en inglés). Este método, que puede realizarse como colgajo de pedículo o colgajo libre, emplea músculo o tejido de la pared inferior del estómago.
-
Colgajo de dorsal ancho. El método de colgajo de pedículo usa músculo y tejido de la parte superior de la espalda. Con frecuencia, los implantes se insertan durante este procedimiento de colgajo.
-
Colgajo de perforantes de las arterias epigástricas inferiores profunda (DIEP, por sus siglas en inglés). El colgajo libre de DIEP toma tejido del abdomen y el cirujano une los vasos sanguíneos a la pared torácica.
-
Colgajo glúteo libre. El colgajo glúteo usa tejidos y músculos de los glúteos para recrear la mama y el cirujano también une los vasos sanguíneos. El colgajo superior transversal del músculo gracilis (TUG, por sus siglas en inglés), que utiliza tejido de la parte superior del muslo, también puede ser una alternativa.
Como en los procedimientos con colgajos intervienen los vasos sanguíneos, por lo general, no se recomiendan estas estrategias para personas con antecedentes de diabetes o de enfermedades en el tejido conectivo o vasculares ni para personas que fuman, ya que el riesgo de problemas durante la cirugía y después de esta son mucho más elevados.
Los procedimientos con colgajos y DIEP son procedimientos más prolongados y el tiempo de recuperación es más prolongado. Sin embargo, es posible que se prefiera el aspecto de la mama, en especial, cuando la radioterapia es parte del plan de tratamiento.
Hable con su médico para obtener más información sobre las opciones de reconstrucción y una derivación a un cirujano plástico. Cuando considere un cirujano plástico, elija a un médico que tenga experiencia en diversas cirugías reconstructivas, incluidos implantes y procedimientos con colgajos, y con quien pueda analizar las ventajas y las desventajas de cada cirugía.
Prótesis mamarias externas
Una prótesis mamaria externa o una prótesis mamaria artificial es una opción para las personas que desean retrasar o no desean someterse a una cirugía reconstructiva (en inglés). Estas pueden ser de silicona o material blando y se encajan en un sostén para mastectomía. Las prótesis mamarias pueden fabricarse de manera que den un aspecto natural y un ajuste bueno. Obtenga más información sobre cómo elegir una prótesis mamaria (en inglés).
Cierre estético plano
Algunas personas eligen un cierre estético plano, también denominada "quedarse plana", después de una mastectomía en vez de cirugia reconstructiva. Esto significa que el cirujano aprieta y alisa la piel, la grasa y el tejido restantes tanto como sea posible para que la pared torácica parezca plana. Sin embargo, quedará una cicatriz.
Si opta por un cierre estético plano después de la mastectomía, es importante elegir a un cirujano que tenga experiencia en la realización del procedimiento. Hable con su cirujano sobre los resultados deseados y pídale ver fotografías de su trabajo. Si no se siente cómodo con la respuesta que recibe, considere obtener una segunda opinión.
Decidir quedarse plana o someterse a una reconstrucción mamaria es una elección personal. Cada persona debe hacer lo que es mejor para ella y elegir lo que honre y respete sus valores y estilo de vida. Obtenga más información en inglés sobre quedarse plana.
Resumen de las opciones de tratamiento quirúrgico
En resumen, las opciones de tratamiento quirúrgico incluyen:
-
Eliminación del cáncer de la mama: lumpectomía o mastectomía parcial, generalmente seguida por radioterapia si el cáncer es invasivo. También se puede recomendar una mastectomía, con o sin reconstrucción inmediata.
-
Evaluación de ganglios linfáticos: biopsia del ganglio linfático centinela o vaciamiento de los ganglios linfáticos axilares.
Se alienta a las pacientes a hablar con sus médicos sobre qué opción quirúrgica es la correcta. Además, hable con el equipo de atención de la salud sobre los posibles efectos secundarios de la cirugía específica a la que se someterá y qué se debe informar.
Una cirugía más extensa, como la mastectomía, no siempre es más conveniente y puede provocar complicaciones adicionales. La combinación de lumpectomía y de radioterapia tiene un riesgo levemente superior de la reaparición de cáncer en la misma mama o en la zona circundante. Sin embargo, la supervivencia a largo plazo de las personas que optan por la lumpectomía es exactamente igual de aquellas que se someten a una mastectomía. Incluso, con una mastectomía, es posible que no se extirpe todo el tejido mamario y existe la posibilidad de recurrencia o de desarrollo de un nuevo cáncer de mama.
Las personas con riesgo muy elevado de desarrollar cáncer en la otra mama pueden considerar una mastectomía bilateral, lo que significa la extirpación de ambas mamas. Esto incluye a personas con mutaciones de los genes BRCA1 y BRCA2 y a personas con cáncer en ambas mamas. Las personas con mutaciones de los genes BRCA1 o BRCA2 deben hablar con su médico sobre qué opción quirúrgica podría ser la mejor para ellas, ya que tienen un mayor riesgo de desarrollar cáncer de mama en la mama opuesta y de desarrollar un nuevo cáncer de mama en la misma mama en comparación con aquellas que no tienen estas mutaciones. La American Society of Clinical Oncology recomienda que también se ofrezca a las personas con una mutación de los genes BRCA1 o BRCA2 que estén siendo tratadas con una mastectomía para la mama con cáncer una mastectomía para reducir el riesgo para la mama opuesta, incluida la mastectomía con conservación del pezón. Esto se debe a que la realización de una mastectomía para reducir el riesgo en la mama opuesta se asocia con una reducción del riesgo de desarrollar cáncer en esa mama. Sin embargo, no todos serán buenos candidatos para la mastectomía con conservación del pezón. Para aquellas con mamas grandes y una pequeña proyección del pezón, por ejemplo, se puede realizar primero una reducción de la mama para conseguir el pezón en una mejor posición.
Para evaluar su riesgo de desarrollar cáncer en la mama opuesta y determinar si podría ser apto para una mastectomía para reducir el riesgo, su médico tendrá en cuenta varios factores:
-
Edad de diagnóstico
-
Antecedentes familiares de cáncer de mama
-
La probabilidad de recurrencia de su cáncer de mama u otros cánceres que pueda tener, como el cáncer de ovario
-
Su capacidad de someterse a estudios de vigilancia regulares, como una RM de mama, para buscar cáncer de mama
-
Cualquier otra enfermedad o afección que pueda tener
-
Esperanza de vida
Las personas con una mutación genética de riesgo moderado, como PALB2, CHEK2 o ATM, también deben hablar con su médico sobre su riesgo de desarrollar cáncer de mama en la mama opuesta y si someterse a una mastectomía para reducir el riesgo, incluida una mastectomía con conservación del pezón, puede ser adecuado para ellas.
Las personas con una mutación de alto riesgo que no se sometan a una mastectomía bilateral deben someterse de forma regular a la detección del tejido mamario restante con una mamografía y RM de la mama anuales para mejorar la vigilancia.
En el caso de las personas que no corran un riesgo muy elevado de presentar un cáncer nuevo en el futuro, la extirpación de una mama saludable en una mastectomía bilateral no evita la recurrencia del cáncer ni mejora su supervivencia. Tampoco cambiará la recomendación para el tratamiento para el cáncer con medicamentos como quimioterapia y terapia hormonal. Si bien se reducirá el riesgo de desarrollar un nuevo cáncer en esa mama, la cirugía para extirpar la otra mama no reduce el riesgo de recurrencia del cáncer original. La supervivencia se basa en el pronóstico del cáncer inicial. Además, una cirugía más amplia puede vincularse con un mayor riesgo de problemas. Obtenga más información sobre cómo hablar con su médico sobre las opciones de cirugía de mama.
Esta información se basa en las recomendaciones de la American Society of Clinical Oncology (en inglés) para el tratamiento para el cáncer de mama hereditario. Tenga en cuenta que este enlace lo llevará a un sitio web diferente de la American Society of Clinical Oncology.
Volver arriba
Radioterapia
La radioterapia es el uso de rayos X u otras partículas con alta potencia para eliminar las células cancerosas. El médico que se especializa en administrar radioterapia para tratar el cáncer se denomina “radioncólogo”. Existen diferentes tipos de radioterapia:
-
Irradiación de toda la mama. La irradiación de toda la mama es una radioterapia de haz externo que se administra a toda la mama. La radioterapia de haz externo es el tipo más común de tratamiento de radiación y se administra desde una máquina fuera del cuerpo. Como se describe a continuación, la irradiación de toda la mama se puede administrar mediante varios programas de tratamiento diferentes.
-
Irradiación parcial de la mama. La irradiación parcial de la mama es la radioterapia que se aplica directamente en el área del tumor en lugar de toda la mama. Es más frecuente después de una lumpectomía. Al dirigir la radiación al área del tumor de forma directa generalmente se reduce el tiempo que las pacientes deben someterse a radioterapia. Sin embargo, solo algunas pacientes pueden ser aptas para recibir irradiación parcial de la mama. Aunque los resultados preliminares han sido prometedores, la irradiación parcial de la mama todavía se encuentra en estudio. La irradiación parcial de la mama puede realizarse con radioterapia con haz externo o radioterapia intraoperatoria o braquiterapia.
-
Radioterapia intraoperatoria. Esto es cuando la radioterapia se administra mediante una sonda en el quirófano.
-
Braquiterapia. Este tipo de radioterapia se administra colocando fuentes radiactivas en el tumor.
Aunque los resultados de las investigaciones son alentadores, la radioterapia intraoperatoria y la braquiterapia no se utilizan ampliamente. Donde estén disponibles, pueden ser opciones para un paciente con un tumor pequeño que no se ha propagado a los ganglios linfáticos. Es posible que desee hablar con su radioncólogo las ventajas y desventajas de la irradiación parcial de la mama en comparación con la radioterapia de toda la mama.
-
Radioterapia de intensidad modulada. La radioterapia de intensidad modulada (IMRT, por sus siglas en inglés) es un método más avanzado para aplicar radioterapia con haz externo en la mama. La intensidad de la radiación dirigida a la mama se modifica para apuntar al tumor con mayor precisión y distribuir de forma más uniforme la radiación en toda la mama. El uso de la IMRT reduce la dosis de radiación y puede disminuir el posible daño a órganos cercanos, como el corazón y el pulmón, y reducir el riesgo de algunos efectos secundarios inmediatos, como la descamación de la piel durante el tratamiento. Esto puede ser particularmente importante para las personas con mamas de tamaño medio a grande, que corren mayor riesgo de sufrir efectos secundarios, como quemaduras y descamación, en comparación con las personas que tienen mamas más pequeñas. La IMRT también puede ayudar a reducir los efectos a largo plazo en el tejido mamario que eran frecuentes con las técnicas de radiación anteriores, como endurecimiento, hinchazón o decoloración.
La IMRT no se recomienda para todas. Hable con su radioncólogo para obtener más información. Para la cobertura de la IMRT, también puede ser necesaria la aprobación de seguro especial. Antes de comenzar cualquier tratamiento, es importante consultar con la aseguradora para asegurarse de que lo cubra.
-
Terapia de protones. La radioterapia estándar para el cáncer de mama usa rayos X, también denominados terapia de fotones, para eliminar las células cancerosas. La terapia de protones es un tipo de radioterapia con haz externo que usa protones en lugar de rayos X. Con alta potencia, los protones pueden destruir las células cancerosas. Los protones poseen distintas propiedades físicas que pueden permitir que la radioterapia sea más dirigida que la terapia de fotones y, posiblemente, reducir la dosis de la radiación. La terapia también puede reducir la cantidad de radiación que llega cerca del corazón. Los investigadores estudian los beneficios de la terapia de protones respecto de la terapia de fotones en un ensayo clínico nacional. En la actualidad, la terapia de protones es un tratamiento experimental y es posible que no esté disponible de manera generalizada o que no esté cubierto por el seguro médico.
Obtenga más información sobre los aspectos básicos de la radioterapia.
Usualmente, un régimen o programa de radioterapia (consulte a continuación) consiste en una cantidad específica de tratamientos que se administran en un período determinado. El tratamiento generalmente se administra una vez al día, 5 días a la semana, durante 1 a 6 meses. Con frecuencia, la radioterapia ayuda a disminuir el riesgo de recurrencia en la mama. De hecho, con la cirugía y la radioterapia modernas, los índices de recurrencia en la mama ahora son menores al 5 % en los 10 años posteriores al tratamiento o del 6 % al 7 % a los 20 años. La supervivencia es la misma con la lumpectomía o mastectomía. Si hay evidencia de cáncer en los ganglios linfáticos debajo del brazo, es posible que también se aplique radioterapia en el cuello o la axila del mismo lado cerca de la mama o la pared torácica.
La radioterapia puede administrarse antes o después de la cirugía:
-
La radioterapia adyuvante se administra después de la cirugía. La mayoría de las pacientes que se someten a una lumpectomía también reciben radioterapia. Es posible que las pacientes a las que se les practica una mastectomía necesiten o no radioterapia, según las características del tumor. Puede recomendarse radioterapia después de la mastectomía si una paciente tiene un tumor más grande, cáncer en los ganglios linfáticos, células cancerosas fuera de la cápsula del ganglio linfático o cáncer que ha crecido hasta afectar la piel o la pared torácica, entre otros motivos. Cuando también se recomienda que las pacientes reciban quimioterapia adyuvante, generalmente se administra radioterapia después de que se completa la quimioterapia. La radioterapia después de la cirugía para CDIS puede o no ofrecerse según el riesgo de recurrencia.
-
La radioterapia neoadyuvante es la radioterapia que se aplica antes de la cirugía para disminuir el tamaño de un tumor grande, lo que facilita su extirpación. Este método es muy poco frecuente y generalmente solo se considera cuando un tumor no se puede extirpar mediante cirugía.
La radioterapia puede causar efectos secundarios, que incluyen fatiga, hinchazón de la mama, enrojecimiento o decoloración de la piel y dolor o ardor en la piel donde se aplicó la radiación, algunas veces con ampollas o descamación. El médico puede recomendar medicamento tópico para aplicar en la piel y tratar algunos de estos efectos secundarios. Después de la radioterapia, la mama puede sentirse más firme o el piel de la mama puede sentirse más gruesa.
En ocasiones muy raras, la radioterapia puede afectar una pequeña parte del pulmón y causar neumonitis, una inflamación del tejido pulmonar relacionada con la radiación. El riesgo depende del tamaño de la zona que recibió la radioterapia y tiende a sanarse con el paso del tiempo.
En el pasado, cuando se utilizaban equipos y técnicas de radioterapia antiguos, las personas que recibían tratamiento para el cáncer de mama del lado izquierdo del cuerpo tenían un leve aumento del riesgo de desarrollar cardiopatía a largo plazo. Las técnicas modernas, como la activación respiratoria, que utiliza tecnología para guiar la administración de radiación mientras el paciente respira, ahora son capaces de evitar que la gran mayoría del corazón tenga los efectos de la radioterapia.
Puede haber muchos tipos de radioterapia disponibles para usted con diferentes programas (consulte a continuación). Hable con el médico sobre las ventajas y las desventajas de cada opción.
Programa de radioterapia
En general, se aplica radioterapia diariamente durante un número determinado de semanas.
-
Después de una lumpectomía. La radioterapia después de una lumpectomía es la radioterapia con haz externo aplicada de lunes a viernes durante 3 a 4 semanas si el cáncer no se encuentra en los ganglios linfáticos. Si el cáncer está en los ganglios linfáticos, la radioterapia se administra durante 5 o 6 semanas. Sin embargo, estas duraciones están cambiando, ya que existe una preferencia por una menor duración en las pacientes que cumplen los criterios para un tratamiento más corto. Esto a menudo incluye radioterapia en toda la mama, seguida de un tratamiento más focalizado en el sitio del tumor en la mama para los tratamientos restantes.
Esta parte focalizada del tratamiento, denominada refuerzo, se realiza de manera rutinaria para la mayoría de pacientes con cáncer de mama invasivo porque reduce el riesgo de una recurrencia en la mama. Las personas con CDIS también pueden recibir el refuerzo. Para las pacientes con bajo riesgo de recurrencia, el refuerzo puede ser opcional. Es importante analizar este enfoque de tratamiento con el médico.
-
Después de una mastectomía. Para quienes necesitan radioterapia después de una mastectomía, esta normalmente se administra 5 días por semana durante 5 a 6 semanas. La radioterapia puede administrarse antes o después de la cirugía reconstructiva. Como es el caso después de una lumpectomía, se puede recomendar a algunas pacientes que se sometan a menos de 5 semanas de radioterapia después de una mastectomía.
Se han estudiado programas aún más breves y algunos centros los están usando, incluyendo la radioterapia parcial acelerada de la mama durante 5 días.
Es posible que estos programas más cortos no representen una opción para las pacientes que necesitan radioterapia después de la mastectomía o radioterapia en los ganglios linfáticos. Asimismo, los programas más prolongados de radioterapia pueden ser necesarios para algunas personas.
Consideraciones sobre la radioterapia adyuvante para pacientes de mayor edad o con tumores pequeños
En estudios de investigación recientes, se ha analizado la posibilidad de no utilizar radioterapia en personas de 65 años o más con un tumor RE positivo, negativo para ganglios linfáticos o en estadio temprano (consulte Introducción) o en aquellas con un tumor de tamaño pequeño. Es importante destacar que estos estudios muestran que, para las personas con tumores de mama pequeños y menos agresivos que se extirpan con lumpectomía, la probabilidad de que el cáncer regrese en la misma mama es muy baja. El tratamiento con radioterapia reduce el riesgo de recurrencia del cáncer de mama en la misma mama incluso más en comparación con la cirugía sola. Sin embargo, la radioterapia no prolonga la vida de una persona.
Las pautas de la National Comprehensive Cancer Network (NCCN, Red Nacional Integral sobre el Cáncer) siguen recomendando la radioterapia como la opción estándar después de la lumpectomía. Sin embargo, indican que las personas que están en situaciones especiales o tienen tumores de bajo riesgo podrían elegir razonablemente no recibir radioterapia y usar solo terapia sistémica con medicamentos (consulte a continuación) después de la lumpectomía. Esto incluye a las personas de 70 años o más o aquellas con otras afecciones médicas que podrían limitar la expectativa de vida a un plazo de 5 años. Las personas que eligen esta opción tendrán un aumento moderado del riesgo de reaparición del cáncer en la mama. Es importante analizar con su médico las ventajas y desventajas de omitir la radioterapia.
Radioterapia adyuvante para quienes tienen una mutación genética
La American Society of Clinical Oncology recomienda (en inglés) que, cuando proceda, se ofrezca radioterapia adyuvante a las personas con cáncer de mama con mutaciones de los genes BRCA1 o BRCA2. Las personas con una mutación del gen TP53 presentan un mayor riesgo de complicaciones por la radioterapia y, por tanto, deberían someterse a una mastectomía en lugar de una lumpectomía y radiación. Las personas con una mutación del gen ATM u otras mutaciones relacionadas deben hablar con su médico sobre si la radioterapia adyuvante es adecuada para ellos. Actualmente no hay suficientes datos para recomendar evitar la radioterapia en todas las personas con mutaciones del gen ATM.
Volver arriba
Terapias con medicamentos
El plan de tratamiento puede incluir medicamentos para destruir las células cancerosas. El medicamento se puede administrar a través del torrente sanguíneo para llegar a las células cancerosas en todo el cuerpo. Cuando un medicamento se administra de esta manera, se le denomina terapia sistémica. El medicamento también se puede administrar a nivel local, que es cuando el medicamento se aplica directamente sobre el cáncer o se mantiene en una sola parte del cuerpo. Sin embargo, esto casi nunca se hace en el tratamiento para el cáncer de mama.
Un oncólogo clínico es quien en general indica este tratamiento, es decir, un médico que se especializa en el tratamiento para el cáncer con medicamentos. Los medicamentos suelen administrarse a través de una vía intravenosa (i.v.) colocada en una vena, como inyección en un músculo o debajo de la piel, o como un comprimido o cápsula que se traga (por vía oral). Si se le administran medicamentos por vía oral, asegúrese de preguntar a su equipo de atención de la salud acerca de cómo conservarlos y manejarlos de forma segura.
Los tipos de medicamentos utilizados para el cáncer de mama incluyen los siguientes:
-
Quimioterapia
-
Terapia hormonal
-
Terapia dirigida
-
Inmunoterapia
Cada una de estas terapias para el tratamiento para el cáncer de mama no metastásico se analiza en más detalle a continuación. Una persona puede recibir 1 tipo de terapia sistémica a la vez o una combinación de medicamentos en forma simultánea. También se pueden administrar como parte de un plan de tratamiento que puede incluir cirugía o radioterapia. Se usan diferentes fármacos o combinaciones de fármacos para tratar la enfermedad metastásica. Puede encontrar información sobre estas terapias en la Guía para el cáncer de mama metastásico de este sitio web.
Los medicamentos utilizados para tratar el cáncer se evalúan constantemente. El médico puede sugerirle considerar participar en ensayos clínicos que estén estudiando métodos nuevos para tratar el cáncer de mama. A menudo, hablar con su médico es la mejor forma de obtener información sobre los medicamentos que le recetaron, su finalidad y sus potenciales efectos secundarios o interacciones con otros medicamentos.
También es importante informar a su médico si está tomando algún otro medicamento con receta o de venta libre, o suplementos. Las hierbas, los suplementos y otros fármacos pueden interactuar con los medicamentos contra el cáncer, lo que provoca efectos secundarios no deseados o una menor eficacia. Obtenga más información sobre sus medicamentos recetados en las bases de datos de fármacos en las que se pueden realizar búsquedas.
Quimioterapia
La quimioterapia es el uso de fármacos para destruir las células cancerosas, generalmente al evitar que las células cancerosas crezcan, se dividan y produzcan más células. Puede administrarse antes de la cirugía para reducir el tamaño de un tumor grande, facilitar la cirugía y disminuir el riesgo de recurrencia. Cuando se administra antes de la cirugía, se denomina “quimioterapia neoadyuvante”. También puede administrarse después de la cirugía para reducir el riesgo de recurrencia, denominada quimioterapia adyuvante.
Un régimen o plan de quimioterapia adyuvante o neoadyuvante normalmente consiste en una combinación de fármacos que se administra en una cantidad específica de ciclos en un plazo determinado. La quimioterapia puede administrarse con muchos programas diversos, según lo que haya funcionado mejor en los ensayos clínicos para ese tipo de régimen en particular. Se puede administrar una vez por semana, una vez cada 2 semanas o una vez cada 3 semanas. Existen muchos tipos de quimioterapia empleados para tratar el cáncer de mama. Los fármacos frecuentes incluyen:
Un paciente puede recibir un fármaco o una combinación de diferentes fármacos administrados al mismo tiempo para tratar el cáncer. Las investigaciones han demostrado que la combinación de determinados fármacos a veces es más eficaz que un fármaco solo para el tratamiento adyuvante.
Los siguientes fármacos o combinaciones de fármacos pueden usarse como terapia adyuvante o neoadyuvante para cáncer de mama de avance local o en estadio temprano:
-
AC (doxorrubicina y ciclofosfamida)
-
EC (epirrubicina y ciclofosfamida)
-
AC o EC seguida de T (paclitaxel o docetaxel), o la inversa
-
AC o EC seguida de T (paclitaxel o docetaxel) y carboplatino, o la inversa
-
CAF (ciclofosfamida, doxorrubicina y 5-FU)
-
CEF (ciclofosfamida, epirrubicina y 5-FU)
-
CMF (ciclofosfamida, metotrexato y 5-FU)
-
TAC (docetaxel, doxorrubicina y ciclofosfamida)
-
TC (docetaxel y ciclofosfamida)
-
Capecitabina (Xeloda)
Las terapias dirigidas al receptor del HER2 pueden administrarse con la quimioterapia para el cáncer de mama HER2 positivo (consulte “Terapia dirigida” a continuación). Un ejemplo es el trastuzumab para anticuerpos. La combinación de regímenes para el cáncer de mama HER2 positivo en un estadio temprano puede incluir:
-
AC-TH (doxorrubicina, ciclofosfamida, paclitaxel o docetaxel, trastuzumab)
-
AC-THP (doxorrubicina, ciclofosfamida, paclitaxel o docetaxel, trastuzumab, pertuzumab)
-
TCH (paclitaxel o docetaxel, carboplatino, trastuzumab)
-
TCHP (paclitaxel o docetaxel, carboplatino, trastuzumab, pertuzumab)
-
TH (paclitaxel, trastuzumab)
Las inmunoterapias se pueden administrar con quimioterapia para el cáncer de mama triple negativo (consulte “Inmunoterapia” a continuación). Un ejemplo es el anticuerpo pembrolizumab. La combinación de regímenes para el cáncer de mama triple negativo puede incluir:
-
TC/pembro-AC/pembro (paclitaxel y carboplatino más pembrolizumab seguidos de doxorrubicina y ciclofosfamida más pembrolizumab)
-
TC/pembro-EC/pembro (paclitaxel y carboplatino más pembrolizumab seguidos de epirrubicina y ciclofosfamida más pembrolizumab)
Los efectos secundarios de la quimioterapia dependen de la persona, de los fármacos utilizados, si se combinó la quimioterapia con otros fármacos y del régimen y la dosis utilizados. Estos efectos secundarios pueden incluir fatiga, riesgo de infección, náuseas y vómitos, caída de cabello, pérdida del apetito, diarrea, estreñimiento, entumecimiento y hormigueo, dolor, menopausia temprana, aumento de peso y quimiocerebro o disfunción cognitiva. Estos efectos secundarios, muchas veces, se pueden prevenir o controlar satisfactoriamente durante el tratamiento con medicamentos de apoyo y, generalmente, desaparecen después de finalizar el tratamiento. Para algunas personas, el entumecimiento y el hormigueo pueden permanecer después de la quimioterapia. Para reducir la caída del cabello, hable con su médico sobre si el centro aplica técnicas de gorro refrigerante. Rara vez, pueden presentarse efectos secundarios a largo plazo, como daño cardíaco o cánceres secundarios, como leucemia o linfoma.
Muchos pacientes se sienten bien durante la quimioterapia y tienen una vida activa cuidando de sus familias, trabajando y ejercitándose durante el tratamiento, aunque las experiencias pueden variar de acuerdo con las personas. Hable con su equipo de atención de la salud sobre los posibles efectos secundarios de su plan de quimioterapia específico y busque atención médica de inmediato si experimenta fiebre durante la quimioterapia.
Obtenga más información sobre los aspectos básicos de la quimioterapia.
Volver arriba
Terapia hormonal
La terapia hormonal, también denominada terapia endocrina, es un tratamiento eficaz para la mayoría de los tumores que dan resultado positivo para los receptores de estrógeno o los receptores de progesterona (denominados “RE positivo” o “RP positivo”; consulte Introducción). Este tipo de tumor usa hormonas para estimular su crecimiento. Bloquear las hormonas puede ayudar a prevenir la recurrencia del cáncer y la muerte por cáncer de mama cuando la terapia hormonal se utiliza ya sea como único tratamiento o después de la quimioterapia.
La terapia hormonal para el tratamiento para el cáncer de mama es diferente de la terapia hormonal menopáusica. La terapia hormonal menopáusica también puede denominarse terapia hormonal posmenopáusica o terapia de reemplazo hormonal. Las terapias hormonales utilizadas en el tratamiento para el cáncer de mama actúan como tratamientos “antihormonales” o “antiestrógenos”. Bloquean las acciones hormonales o los niveles hormonales más bajos en el organismo. A la terapia hormonal también se la denomina terapia endocrina. El sistema endocrino del organismo produce hormonas. Obtenga más información sobre los aspectos básicos de la terapia hormonal.
Se puede administrar terapia hormonal antes de la cirugía para reducir un tumor, facilitar la cirugía o disminuir el riesgo de recurrencia. Esto se denomina “terapia hormonal neoadyuvante”. Cuando se administra antes de la cirugía, normalmente se administra durante al menos de 3 a 6 meses antes de la cirugía y continúa después de la cirugía. También puede administrarse únicamente después de la cirugía para reducir el riesgo de recurrencia. Denominamos a esto terapia hormonal adyuvante.
Tipos de terapia hormonal
-
Tamoxifeno. El tamoxifeno es un medicamento que bloquea la fijación del estrógeno a las células mamarias cancerosas. Resulta eficaz para reducir el riesgo de recurrencia en la mama que tenía cáncer, el riesgo de desarrollar cáncer en la otra mama y el riesgo de recurrencia a distancia. El tamoxifeno funciona bien en personas que han transitado la menopausia y en aquellas que no.
El tamoxifeno es una píldora que se toma diariamente por vía oral todos los días durante 5 a 10 años. Para las personas premenopáusicas, se puede combinar con medicamentos para evitar que los ovarios produzcan estrógeno. Es importante que analice con el médico cualquier otro medicamento o suplemento que use, dado que existen algunos que interfieren con el tamoxifeno. Los efectos secundarios frecuentes del tamoxifeno incluyen sofocos y sequedad, secreción o sangrado vaginales. Riesgos muy raros incluyen cáncer de la pared interior del útero, cataratas y coágulos sanguíneos. Sin embargo, el tamoxifeno puede mejorar la salud ósea y los niveles de colesterol en personas posmenopáusicas.
-
Inhibidores de la aromatasa (IA). Los IA disminuyen la cantidad de estrógeno producido por los tejidos que no son de los ovarios en las personas posmenopáusicas al bloquear la enzima aromatasa. Esta enzima cambia las hormonas masculinas débiles, denominadas andrógenos, a estrógenos. Entre estos medicamentos se incluyen el anastrozol (Arimidex), el exemestano (Aromasin) y el letrozol (Femara). Todos los IA son pastillas que se toman diariamente por vía oral. Solo las pacientes que transitaron la menopausia o que tomaron medicamentos para evitar que los ovarios elaboren estrógeno (consulte “Supresión ovárica” a continuación) pueden tomar IA. El tratamiento con IA, ya sea como primera terapia hormonal recibida o después del tratamiento con tamoxifeno, puede ser más efectivo que tomar solo tamoxifeno para reducir el riesgo de recurrencia en las personas posmenopáusicas.
Los efectos secundarios de los IA pueden incluir dolor articular y muscular, sofocos, sequedad vaginal, un mayor riesgo de osteoporosis y fracturas de los huesos, y, con poca frecuencia, aumentos en los niveles del colesterol. Las investigaciones demuestran que todos los IA funcionan igual de bien y tienen efectos secundarios similares. Sin embargo, las personas que tienen efectos secundarios no deseados mientras están tomando un IA pueden tener menos efectos secundarios con otro IA por razones poco claras.
Las pacientes que no han pasado la menopausia y que no están recibiendo inyecciones para impedir que los ovarios funcionen (consulte a continuación) no deben tomar IA, ya que no bloquean los efectos del estrógeno producido por los ovarios. A menudo, los médicos monitorearán los niveles de estrógeno en la sangre en personas cuyos ciclos menstruales han cesado, cuyos períodos cesaron con la quimioterapia o a quienes se les ha hecho una histerectomía, pero que conservan los ovarios para asegurarse de que los ovarios ya no están produciendo estrógeno.
-
Ablación o supresión ovárica. La supresión ovárica se trata del uso de fármacos para evitar que los ovarios produzcan estrógeno. La ablación ovárica es el uso de la cirugía para extirpar los ovarios. Estas opciones pueden usarse además de otro tipo de terapia hormonal para personas que no transitaron la menopausia.
-
En el caso de la supresión ovárica, se utilizan fármacos agonistas de la hormona liberadora de gonadotropina u hormona liberadora de la hormona luteinizante (GnRH o LHRH) para detener la producción de estrógeno en los ovarios, lo cual ocasiona una menopausia temporal. La goserelina (Zoladex) y la leuprolida (Eligard, Lupron) son tipos de estos fármacos. Generalmente se administran en combinación con otra terapia hormonal, no solos. Se administran por inyección cada 4 o 12 semanas y evitan que los ovarios generen estrógeno. Los efectos de los fármacos GnRH desaparecen si se interrumpe el tratamiento.
-
En el caso de la ablación ovárica, la cirugía para extirpar los ovarios se usa para detener la producción de estrógeno. Si bien esto es permanente, puede ser una buena opción para las personas que ya no desean quedar embarazadas. El costo suele ser más bajo a largo plazo.
Terapia hormonal después de la menopausia
Las personas que han pasado por la menopausia y a quienes se les receta terapia hormonal cuentan con diversas opciones:
-
Tamoxifeno durante 5 a 10 años.
-
Un IA durante un período de 5 a 10 años.
-
Tamoxifeno durante 5 años, seguido de un IA hasta un máximo de 5 años. Esto será un total de 10 años de terapia hormonal.
-
Tamoxifeno durante un período de 2 a 3 años, seguido de 2 a 8 años de un IA durante un total de 5 a 10 años de terapia hormonal.
En general, las pacientes deben esperar recibir de 5 a 10 años de terapia hormonal. Los biomarcadores tumorales y otras características del cáncer también pueden afectar a quien se recomienda recibir una tanda más prolongada de terapia hormonal.
Terapia hormonal antes de la menopausia
Como se indicó anteriormente, las pacientes premenopáusicas no deben tomar IA sin supresión ovárica, ya que no disminuirán los niveles de estrógeno. Las opciones de terapia hormonal adyuvante para personas premenopáusicas incluyen las siguientes:
-
Tamoxifeno durante 5 años. Luego, el tratamiento se basa en su riesgo de recurrencia del cáncer, así como en si han atravesado la menopausia durante esos primeros 5 años o no.
-
Si una persona no transitó la menopausia después de los primeros 5 años de tratamiento y se recomienda continuarlo, podrá continuar con el tamoxifeno durante otros 5 años, durante un total de 10 años de tamoxifeno. De manera alternativa, una persona podría comenzar la supresión ovárica y cambiar a tomar un IA durante otros 5 años.
-
Si una persona transita la menopausia durante los primeros 5 años de tratamiento y se recomienda continuarlo, podrá continuar con el tamoxifeno durante 5 años más o cambiar a un IA durante otros 5 años. Esto será un total de 10 años de terapia hormonal. Solo las personas que claramente sean posmenopáusicas deberán considerar tomar un IA.
-
Se recomienda que algunas pacientes interrumpan toda terapia hormonal después de los primeros 5 años de tamoxifeno.
-
Podrá recomendarse la supresión ovárica durante 5 años junto con una terapia hormonal adicional, como el tamoxifeno o un IA, en las siguientes situaciones, según la edad de la persona y el riesgo de recurrencia:
-
En el caso de personas diagnosticadas con cáncer de mama a edad muy temprana.
-
En el caso de personas con alto riesgo de recurrencia del cáncer.
-
En el caso de personas con cáncer en estadio II o III cuando también se recomiende quimioterapia. Sin embargo, la evidencia actual sugiere beneficios independientes del uso de la quimioterapia también.
-
En el caso de personas con cáncer en estadio I o II con un mayor riesgo de recurrencia, que también puedan evaluar someterse a quimioterapia.
-
En el caso de personas que no puedan tomar tamoxifeno por otros motivos de salud, como tener antecedentes de coágulos de sangre. Tomaban un IA además de la supresión ovárica.
-
No se recomienda la supresión ovárica además de otro tipo de terapia hormonal en las siguientes situaciones:
Terapia dirigida adicional en combinación con terapia hormonal
El siguiente fármaco se utiliza en combinación con terapia hormonal para el tratamiento del cáncer de mama no metastásico positivo para receptores hormonales y negativo para HER2, y un riesgo elevado de recurrencia del cáncer de mama.
-
Abemaciclib (Verzenio). Este fármaco oral, denominado “inhibidor de CDK4/6”, apunta a una proteína en las células mamarias cancerosas llamada “CDK4/6”, la cual puede estimular el crecimiento de células cancerosas. Está aprobado como tratamiento en combinación con terapia hormonal (tamoxifeno o un IA) para tratar a personas con cáncer de mama en estadio temprano, positivo para receptores hormonales y negativo para HER2 que se ha diseminado a los ganglios linfáticos y tiene un alto riesgo de recurrencia. Puede causar diarrea, recuento sanguíneo bajo, fatiga y otros síntomas. La American Society of Clinical Oncology recomienda (en inglés) considerar 2 años de tratamiento con abemaciclib combinado con 5 o más años de terapia hormonal para las pacientes que cumplan con estos criterios, incluidas las personas cuyo cáncer tenga un índice de Ki-67 superior al 20 % (consulte Diagnóstico).
Esta información está basada en las recomendaciones de la American Society of Clinical Oncology sobre la terapia endocrina adyuvante para mujeres con cáncer de mama positivo para el receptor de hormonas. Tenga en cuenta que este enlace lo llevará a otro sitio web en inglés de la American Society of Clinical Oncology.
La terapia hormonal para el tratamiento para el cáncer de mama metastásico positivo para receptores hormonales se describe en la Guía para el cáncer de mama metastásico.
Obtenga más información sobre los aspectos básicos de la terapia hormonal.
Volver arriba
Terapia dirigida
La terapia dirigida es un tratamiento que apunta a los genes, las proteínas o las condiciones del tejido que contribuyen al crecimiento y la supervivencia del cáncer. Estos tratamientos son muy focalizados y son distintos de la quimioterapia. Este tipo de tratamiento bloquea el crecimiento y la diseminación de las células cancerosas y limita el daño a las células sanas.
No todos los tumores tienen los mismos objetivos. Para determinar cuál es el tratamiento más eficaz, el médico puede realizar pruebas para identificar los genes, las proteínas y otros factores involucrados en el tumor. Además, continúan realizándose estudios de investigación para obtener más información sobre objetivos moleculares específicos y tratamientos nuevos dirigidos a ellos. Obtenga más información sobre los aspectos básicos de los tratamientos dirigidos.
Las primeras terapias dirigidas aprobadas para el cáncer de mama fueron las terapias hormonales. Luego, se aprobaron las terapias dirigidas al HER2 para tratar el cáncer de mama con HER2 positivo.
Terapia dirigida a HER2
-
Trastuzumab (están disponibles las formas biosimilares aprobados por la FDA). Este fármaco está aprobado como terapia para el cáncer de mama HER2 positivo no metastásico. Se administra como infusión en una vena cada 1 a 3 semanas o como inyección en la piel cada 3 semanas. Actualmente, las pacientes con cáncer de mama en estadios de I a III (consulte Estadios) deben recibir un régimen basado en trastuzumab que a menudo incluye una combinación de trastuzumab con quimioterapia seguida de un año de terapia dirigida a HER2 adyuvante. Las pacientes que reciben trastuzumab tienen un pequeño riesgo (del 2 % al 5 %) de desarrollar problemas cardíacos. Este riesgo aumenta si una paciente tiene otros factores de riesgo para la cardiopatía o recibe quimioterapia que también aumenta el riesgo de desarrollar problemas cardíacos al mismo tiempo. Estos problemas cardíacos pueden desaparecer y pueden tratarse con medicamentos.
-
Pertuzumab (Perjeta). Este fármaco está aprobado para el cáncer de mama en estadios II y III en combinación con trastuzumab y quimioterapia. Se administra como infusión en una vena cada 3 semanas.
-
Pertuzumab, trastuzumab e hialuronidasa-zzxf (Phesgo). Este fármaco combinado, que contiene pertuzumab, trastuzumab y hialuronidasa-zzxf en una dosis única, está aprobado para personas con cáncer de mama de estadio temprana HER2 positivo. Puede administrarse en combinación con quimioterapia. Se administra mediante inyección debajo de la piel y puede ser administrada en un centro de tratamiento o en su casa por un profesional de atención médica.
-
Neratinib (Nerlynx). Este fármaco oral está aprobado como tratamiento para el cáncer de mama HER2 positivo en un estadio temprano de mayor riesgo. Se toma durante un año, a partir de que las pacientes completaron un año de trastuzumab.
-
Ado-trastuzumab emtansina o T-DM1 (Kadcyla). Está aprobado para las pacientes con cáncer de mama en estadio temprano que han recibido tratamiento con trastuzumab y quimioterapia con paclitaxel o docetaxel seguido de cirugía, y que han tenido cáncer restante (o presente) al momento de la cirugía. La American Society of Clinical Oncology recomienda (en inglés) que estas pacientes reciban 14 ciclos de T-DM1 después de la cirugía, a menos que el cáncer reaparezca o que los efectos secundarios de T-DM1 se tornen demasiado difíciles de manejar. T-DM1 es una combinación de trastuzumab vinculado con una cantidad muy pequeña de una quimioterapia fuerte. Esto permite que el fármaco administre quimioterapia en la célula cancerosa mientras disminuye la quimioterapia recibida por las células sanas, lo que generalmente significa que causa menos efectos secundarios que la quimioterapia estándar. La T-DM1 se administra por vía intravenosa cada 3 semanas.
Esta información se basa en la guía de la American Society of Clinical Oncology, “Selección de quimioterapia adyuvante óptima y terapia dirigida para el cáncer de mama temprano”. Tenga en cuenta que este enlace lo llevará a otro sitio web en inglés de la American Society of Clinical Oncology.
Hable con el médico sobre los posibles efectos secundarios de los medicamentos específicos y sobre cómo se pueden manejar.
Fármacos modificadores óseos
Los fármacos modificadores óseos bloquean la destrucción ósea y ayudan a fortalecer los huesos. Estos medicamentos, denominados bisfosfonatos, también se pueden usar para prevenir la recurrencia del cáncer en los huesos. Los fármacos modificadores óseos no sustituyen los tratamientos antineoplásicos estándares. Algunos tipos de fármacos modificadores óseos también se usan en bajas dosis para prevenir y tratar la osteoporosis, que es el afinamiento de los huesos.
Todas las personas con cáncer de mama que han pasado por la menopausia, independientemente del estado de receptores hormonales y el estado de HER2 del cáncer, deben analizar con su médico si los bisfosfonatos son adecuados para ellos. Varios factores afectan esta decisión, incluido su riesgo de recurrencia, los efectos secundarios del tratamiento, el costo del tratamiento, sus preferencias y su salud general.
Si se recomienda el tratamiento con bisfosfonatos, la American Society of Clinical Oncology recomienda comenzar dentro de los 3 meses posteriores a la cirugía o dentro de los 2 meses posteriores a la quimioterapia adyuvante. Esto puede incluir tratamiento con clodronato (marcas múltiples), ibandronato (Boniva) o ácido zoledrónico (Zometa). El clodronato no se encuentra disponible en Estados Unidos.
Esta información se basa en la guía de la American Society of Clinical Oncology y Ontario Health (Cancer Care Ontario), “Uso de bisfosfonatos adyuvantes y otros agentes modificadores de los huesos en el cáncer de mama”. Tenga en cuenta que este enlace lo llevará a otro sitio web en inglés de la American Society of Clinical Oncology.
Otros tipos de terapia dirigida para el cáncer de mama
Es posible que tenga otras opciones de terapias dirigidas para el tratamiento para el cáncer de mama, de acuerdo con varios factores. El siguiente fármaco se utiliza para el tratamiento para el cáncer de mama no metastásico en personas con una mutación hereditaria de los genes BRCA1 o BRCA2 y un alto riesgo de recurrencia del cáncer de mama.
- Olaparib (Lynparza). Es un tipo de fármaco oral denominado inhibidor de PARP, que destruye las células cancerosas al impedirles la corrección del daño a las células. La American Society of Clinical Oncology recomienda (en inglés) el uso de olaparib para tratar el cáncer de mama HER2 negativo en estadio temprano en personas con una mutación hereditaria de los genes BRCA1 o BRCA2 y un alto riesgo de recurrencia del cáncer de mama. El olaparib adyuvante debe administrarse durante 1 año después de la finalización de la quimioterapia, cirugía y radioterapia (si es necesario).
Puede obtener más información sobre los fármacos utilizados para tratar el cáncer de mama metastásico en la Guía para el cáncer de mama metastásico.
Volver arriba
Inmunoterapia
La inmunoterapia utiliza las defensas naturales del cuerpo para combatir el cáncer al mejorar la capacidad de su sistema inmunitario para atacar las células cancerosas. El siguiente fármaco, que es un tipo de inmunoterapia denominada “inhibidor del punto de control inmunitario”, se usa para el tratamiento para el cáncer de mama triple negativo, en estadio temprano y de alto riesgo.
- Pembrolizumab (Keytruda). Este es un tipo de inmunoterapia que está aprobada por la FDA para tratar el cáncer de mama triple negativo, en estadio temprano y de alto riesgo en combinación con quimioterapia antes de la cirugía. Luego, se continúa después de la cirugía por 9 dosis.
Los efectos secundarios frecuentes incluyen erupciones cutáneas, síntomas similares a la gripe, problemas en la glándula tiroidea, diarrea y cambios de peso. También pueden producirse otros efectos secundarios graves, pero menos frecuentes. Hable con su médico sobre los posibles efectos secundarios de la inmunoterapia recomendada para usted y qué se puede hacer para vigilarlos y controlarlos. Obtenga más información sobre los aspectos básicos de la inmunoterapia.
Volver arriba
Terapia sistémica neoadyuvante para el cáncer de mama no metastásico
La terapia sistémica neoadyuvante es el tratamiento administrado antes de la cirugía para reducir el tamaño de un tumor grande o reducir el riesgo de recurrencia. La quimioterapia, la inmunoterapia, la terapia hormonal y la terapia dirigida pueden administrarse como tratamientos neoadyuvantes para personas con ciertos tipos de cáncer de mama.
Por ejemplo, la quimioterapia neoadyuvante es el tratamiento que generalmente se recomienda para las personas con cáncer de mama inflamatorio (en inglés). También es el tratamiento recomendado para las personas con cáncer de avance local (tumores grandes o varios ganglios linfáticos afectados) o cáncer que sería difícil de extirpar con cirugía al momento del diagnóstico, pero que puede ser extirpable con cirugía después de recibir tratamiento neoadyuvante. El médico considerará varios factores, incluido el tipo de cáncer de mama que usted tiene —como su grado, estadio y estado de estrógeno, progesterona y HER2— para guiar su recomendación sobre si la quimioterapia neoadyuvante debe ser parte de su plan de tratamiento.
La American Society of Clinical Oncology recomienda que la terapia sistémica neoadyuvante se ofrezca a personas con cáncer de mama HER2 positivo de alto riesgo o a personas con cáncer de mama triple negativo que luego recibirían otra terapia farmacológica después de la cirugía si el cáncer continúa. La terapia neoadyuvante también puede ofrecerse para reducir la cantidad de cirugías que se deben realizar y permitir que alguien que, de otro modo, requeriría una mastectomía, por ejemplo, considere someterse a una lumpectomía.
En situaciones en las que no se pueda evitar o se prefiera retrasar la cirugía (como esperar los resultados de las pruebas genéticas para fundamentar más opciones de tratamiento o para dar tiempo para decidir sobre las opciones de reconstrucción mamaria), se puede ofrecer terapia sistémica neoadyuvante.
Las personas que reciben quimioterapia neoadyuvante deben ser monitoreadas para detectar la respuesta del cáncer al tratamiento mediante exámenes regulares. Es probable que su médico sugiera estudios de diagnóstico por imágenes de mama después del tratamiento para la planificación quirúrgica. También puede realizar estudios por imágenes si cree que el cáncer puede haber progresado a pesar del tratamiento. Su médico probablemente usará el mismo tipo de prueba de diagnóstico por imágenes en su atención de seguimiento que fue más útil en el momento en que se le diagnosticó originalmente el cáncer de mama. En general, no se recomienda el uso de análisis de sangre o biopsias para monitorear la respuesta a la terapia en personas que reciben quimioterapia neoadyuvante.
Opciones de terapia sistémica neoadyuvante por tipo de cáncer de mama no metastásico
Para el cáncer de mama triple negativo:
En el caso de las pacientes con cáncer de mama triple negativo que se ha diseminado a los ganglios linfáticos o tiene un tamaño de más de 1 centímetro (cm), la American Society of Clinical Oncology recomienda que se les ofrezca quimioterapia neoadyuvante. También se pueden recomendar otros fármacos, incluido el medicamento de quimioterapia carboplatino y el medicamento de inmunoterapia pembrolizumab (consulte más arriba), además de los medicamentos de quimioterapia habituales para aumentar la probabilidad de tener una respuesta completa y reducir el riesgo de reaparición del cáncer. Se produce una respuesta completa cuando no se encuentra cáncer en el tejido cuando se extirpa durante la cirugía. Hable con su médico sobre los posibles beneficios y riesgos de recibir carboplatino y pembrolizumab antes de la cirugía.
No se debe ofrecer terapia neoadyuvante de rutina a las personas con cáncer de mama triple negativo en estadio temprano (1 cm o menos y sin ganglios linfáticos que parezcan anómalos), a menos que estén participando en un ensayo clínico.
Para el cáncer de mama con receptor hormonal positivo, HER2 negativo:
En los casos en los que se puede hacer una recomendación de quimioterapia sin contar con toda la información obtenida de la cirugía, como el tamaño real del tumor o la cantidad de ganglios linfáticos afectados, cualquier persona con cáncer de mama HER2 negativo y positivo para receptores hormonales puede recibir quimioterapia neoadyuvante en lugar de quimioterapia adyuvante. Mientras tanto, para las personas posmenopáusicas con tumores grandes u otros motivos por los que la cirugía puede no ser una buena opción en el momento del diagnóstico del cáncer, se puede ofrecer terapia hormonal con un inhibidor de la aromatasa para reducir el tamaño del tumor. También se puede usar para controlar el cáncer si no cumple ningún rol para la cirugía. Sin embargo, la terapia hormonal no debe ofrecerse en forma rutinaria en esta situación fuera de un ensayo clínico para personas premenopáusicas con cáncer de mama HER2 negativo, en etapa temprana y positivo para receptores hormonales.
Para el cáncer de mama HER2 positivo:
Para pacientes con cáncer de mama HER2 positivo que se ha diseminado a los ganglios linfáticos o tiene más de 2 cm de tamaño, debe ofrecerse terapia neoadyuvante con quimioterapia en combinación con el medicamento de terapia dirigida trastuzumab. Otro medicamento de terapia dirigida contra el HER2, pertuzumab, también puede usarse con trastuzumab cuando se administra antes de la cirugía. Sin embargo, a las personas con cáncer en estadio temprano (1 cm o menor y sin aparición de ganglios linfáticos anómalos), HER2 positivo, no se les debe ofrecer quimioterapia neoadyuvante de rutina ni medicamentos dirigidos al HER2 (como trastuzumab y pertuzumab) fuera de un estudio clínico.
Esta información se basa en la guía de la American Society of Clinical Oncology, “Quimioterapia neoadyuvante, terapia endocrina y terapia dirigida para el cáncer de mama”. Tenga en cuenta que este enlace lo llevará a otro sitio web en inglés de la American Society of Clinical Oncology.
Volver arriba
Inquietudes sobre la terapia sistémica para personas de 65 años o más
La edad nunca debería ser el único factor empleado para determinar las opciones de tratamiento. Los tratamientos sistémicos, como la quimioterapia, a menudo funcionan tan bien en pacientes de mayor edad como lo hacen en las más jóvenes. Sin embargo, las pacientes de mayor edad pueden tener más probabilidades de presentar efectos secundarios que afecten su calidad de vida. Las pacientes mayores también pueden tener un mayor riesgo de toxicidades asociadas con el medicamento.
Por ejemplo, las pacientes de mayor edad pueden correr un mayor riesgo de desarrollar problemas cardíacos por el trastuzumab. Esto es más frecuente en el caso de pacientes que ya padecen cardiopatía y en el de quienes reciben ciertas combinaciones de quimioterapia. En el caso de las pacientes mayores que reciben quimioterapia, pueden tener un mayor riesgo de fatiga y neuropatía periférica. Obtenga más información en este artículo separado en este sitio web.
Es importante que todas las pacientes hablen con sus médicos sobre las opciones recomendadas de terapia sistémica, incluidos los beneficios y los riesgos. También deben preguntar acerca de los posibles efectos secundarios, y cómo pueden controlarse. Obtenga más información sobre el cáncer y el envejecimiento.
Volver arriba
Efectos físicos, emocionales y sociales del cáncer
En general, el cáncer y su tratamiento producen síntomas y efectos secundarios físicos, así como efectos emocionales, sociales y económicos. El manejo de estos efectos se denomina cuidados paliativos o atención médica de apoyo. Es una parte importante de su atención que se incluye junto con los tratamientos que tienen como fin retrasar, detener o eliminar el cáncer.
El tratamiento de apoyo se centra en mejorar cómo se siente durante el tratamiento al manejar los síntomas y brindar apoyo a las pacientes y sus familias con otras necesidades no médicas. Cualquier persona, independientemente de la edad o del tipo y estadio de cáncer, puede recibir este tipo de atención. Y en general, funciona mejor cuando se inicia poco después del diagnóstico de cáncer. Las personas que reciben tratamiento de apoyo junto con el tratamiento para el cáncer con frecuencia tienen síntomas menos graves y mejor calidad de vida, e informan que están más satisfechas con el tratamiento.
Los tratamientos de apoyo varían ampliamente y, con frecuencia, incluyen medicamentos, cambios nutricionales, técnicas de relajación, apoyo emocional y espiritual, y otras terapias.
Las investigaciones demuestran que algunas terapias integradoras o complementarias podrían resultar útiles para controlar los síntomas y los efectos secundarios. La medicina integradora es aquella que combina el uso del tratamiento médico para el cáncer junto con terapias complementarias, como las prácticas mente-cuerpo, los productos naturales o los cambios en el estilo de vida. Sin embargo, la mayoría de los productos naturales no están regulados, por lo que el riesgo de que interactúen con su tratamiento y provoquen daños es incierto. La American Society of Clinical Oncology acepta las recomendaciones de la Society for Integrative Oncology (Sociedad de Oncología Integradora) sobre varias opciones complementarias para ayudar a controlar los efectos secundarios durante y después del tratamiento para el cáncer de mama. Estos incluyen las siguientes:
-
Musicoterapia, meditación, manejo del estrés y yoga para reducir la ansiedad y el estrés.
-
Meditación, relajación, yoga, masajes y musicoterapia para la depresión y para mejorar otros problemas de ánimo.
-
Meditación y yoga para mejorar la calidad de vida en general.
-
Acupresión y acupuntura para ayudar con las náuseas y los vómitos de la quimioterapia.
Obtenga más información sobre las recomendaciones de terapia integradora para controlar los efectos secundarios del cáncer de mama y su tratamiento en un sitio web diferente en inglés de la American Society of Clinical Oncology.
Las personas pueden tener inquietudes respecto de si su tratamiento puede afectar su salud sexual y su capacidad para tener hijos en el futuro, lo cual se denomina “fertilidad”. Se recomienda a las personas que hablen con el equipo de atención de la salud sobre estos temas antes de comenzar el tratamiento.
Antes de comenzar con el tratamiento, hable con su médico sobre los objetivos de cada tratamiento en el plan de tratamiento recomendado. También debe hablar sobre los efectos secundarios posibles del plan de tratamiento específico y las opciones de manejo de los síntomas. Muchas personas también se benefician al hablar con un trabajador social y participar en grupos de apoyo. Pregúntele también a su médico sobre estos recursos.
Durante el tratamiento, su equipo de atención de la salud puede pedirle que responda preguntas sobre sus síntomas y efectos secundarios, y que describa cada problema. Asegúrese de informar al equipo de atención de la salud si experimenta algún problema. Esto ayuda a que el equipo de atención de la salud pueda tratar cualquier síntoma y efecto secundario lo más rápido posible. También puede ayudar a prevenir problemas más graves en el futuro.
Obtenga más información sobre la importancia de llevar un registro de los efectos secundarios en otra parte de esta guía. Obtenga más información sobre el tratamiento de apoyo o los cuidados paliativos en una sección diferente de este sitio web.
Volver arriba
Cáncer de mama recurrente
Si el cáncer regresa después del tratamiento para la enfermedad en estadio temprano, recibe el nombre de cáncer recurrente. Cuando el cáncer de mama es recurrente, puede reaparecer en las siguientes partes del cuerpo:
-
El mismo lugar que el cáncer original. Esto se denomina “recurrencia local”.
-
En la pared torácica o los ganglios linfáticos debajo del brazo o en el tórax en el mismo lado del cáncer original. Esto se denomina “recurrencia regional”.
-
En otro lugar, incluidos órganos distantes, tales como los huesos, los pulmones, el hígado y el cerebro. Esto se denomina “recurrencia distante o recurrencia metastásica”. Para obtener más información sobre recurrencia metastásica, consulte la Guía de cáncer de mama metastásico.
Cuando se da una recurrencia, comenzará nuevamente un nuevo ciclo de pruebas para obtener la mayor cantidad de información posible sobre ella. Las pruebas pueden incluir diagnósticos por imágenes, tales como lo analizado en la sección Diagnóstico. Además, es posible que sea necesario realizar otra biopsia a fin de confirmar la recurrencia del cáncer de mama y obtener más información sobre las características del cáncer.
Después de realizadas estas pruebas, usted y su médico hablarán sobre sus opciones de tratamiento. El plan de tratamiento puede incluir los tratamientos descritos anteriormente, tales como cirugía, radioterapia, quimioterapia, terapia dirigida y terapia hormonal. Quizás se combinen de un modo diferente o se administren con un ritmo distinto. Las opciones de tratamiento para el cáncer de mama recurrente dependen de los siguientes factores:
-
Tratamientos previos para el cáncer diagnosticado por primera vez.
-
Tiempo desde el primer diagnóstico.
-
Ubicación de la recurrencia.
-
Características del tumor, tales como estado del RE, RP y HER2.
-
Resultados de análisis genómicos previos.
-
Según el tipo de cáncer de mama, es posible que su médico le recomiende hacerse las siguientes pruebas de detección de características moleculares:
-
PD-L1. En la superficie de las células cancerosas y en algunas células inmunitarias del cuerpo, se encuentra el ligando de muerte programada-1 (PD-L1, por sus siglas en inglés). Esta proteína impide que las células inmunitarias del cuerpo destruyan al cáncer, especialmente el cáncer de mama triple negativo.
-
Inestabilidad de microsatélites alta (IMS-A) o deficiencia en la reparación de errores de emparejamiento (MMR). Los tumores que tienen inestabilidad de microsatélites alta (IMS-A) o deficiencia en la reparación de errores de emparejamiento (MMR) tienen dificultades para reparar el daño en su ADN. Esto significa que desarrollan muchas mutaciones o cambios. Estos cambios producen proteínas anormales en las células tumorales que hacen que sea más fácil para las células inmunitarias encontrar y atacar el tumor.
-
Fusiones del gen NTRK. Es un cambio genético específico encontrado en varios tipos de cáncer, incluido el cáncer de mama.
-
Mutación del gen PI3KCA. Este es un cambio genético específico que se halla comúnmente en el cáncer de mama.
Las personas con cáncer de mama recurrente en ocasiones sienten emociones como incredulidad o temor. Es recomendable que hable con su equipo de atención de la salud respecto de estos sentimientos y que solicite servicios de apoyo que la ayuden a sobrellevar la situación. Obtenga más información sobre cómo afrontar la recurrencia del cáncer.
Opciones de tratamiento para una recurrencia de cáncer de mama local o regional
Una recurrencia local o regional, a menudo, puede manejarse y puede ser curable. Las opciones de tratamiento se explican a continuación:
-
Para las personas que presentan una recurrencia local en la mama después del tratamiento inicial con lumpectomía y radioterapia adyuvante, el tratamiento recomendado es, por lo general, la mastectomía. Generalmente, el cáncer se extirpa completamente con este tratamiento.
-
Para personas con recurrencia local o regional en la pared torácica después de una mastectomía inicial, la extirpación quirúrgica de la recurrencia seguida de radioterapia en la pared torácica y los ganglios linfáticos es el tratamiento recomendado. No obstante, si ya se ha administrado radioterapia para el cáncer inicial, esta no puede ser una opción. La radioterapia por lo general no puede administrarse en dosis completa en la misma zona más de una vez. Algunas veces se aplica terapia sistémica antes de la cirugía para disminuir el tamaño del cáncer y facilitar la extirpación.
-
Otros tratamientos que se emplean para reducir las posibilidades de una recurrencia distante futura comprenden radioterapia, quimioterapia, terapia hormonal y terapia dirigida. Estas se usan en función del tumor y del tipo de tratamiento que se utilizó previamente.
Sea cual sea el plan de tratamiento que usted elija, los cuidados paliativos serán importantes para aliviar los síntomas y los efectos secundarios. El médico puede sugerirle ensayos clínicos que estén estudiando métodos nuevos para tratar el cáncer de mama recurrente.
Volver arriba
La siguiente sección de esta guía es Acerca de los ensayos clínicos. Ofrece más información sobre los estudios de investigación que se centran en buscar mejores maneras de atender a las personas con cáncer de mama. Use el menú para elegir una sección diferente para leer en esta guía.